|
|
面对实体瘤“难到达、难穿透、难治透”的世界性难题,复旦大学孔彪、江立波、董健团队交出了一项兼具原创性与转化潜力的最新成果:一种能够深度穿透实体瘤的智能介孔纳米环。1 i: L/ `" E `6 k( z
这项研究的灵感,来自自然界的“造物方式”。硅藻和海绵等生物体内精细复杂的硅结构,并不是用固定模具“压”出来的,而是在动态变化的微环境中一步步“长”出来的。复旦大学团队正是借鉴这一自然过程,提出凝聚体导向的硅化新策略,成功实现六角有序介孔纳米环的可控构建。
' }7 P4 i8 e" T! X, f6 U" j
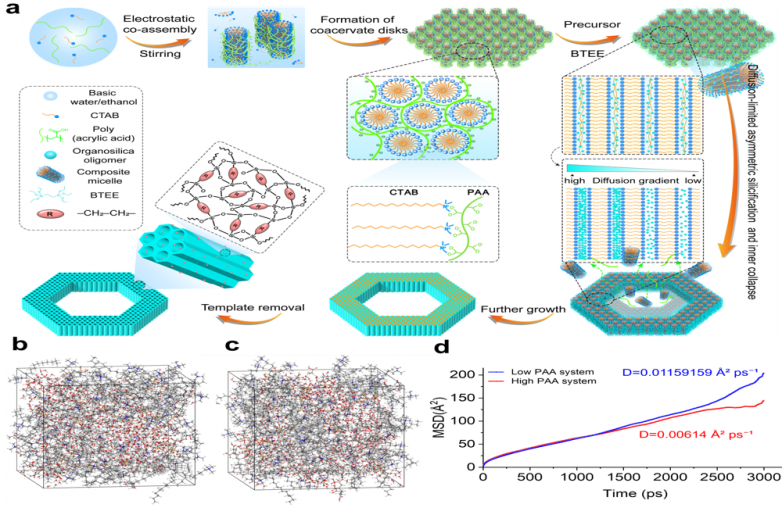 图1 扩散受限非平衡硅化驱动的环形拓扑形成机制 : i) @: q+ O0 P$ H
图1 扩散受限非平衡硅化驱动的环形拓扑形成机制 : i) @: q+ O0 P$ H
长期以来,传统介孔材料更容易形成球形、棒状等规则对称结构,而像环形这样更复杂的拓扑往往难以自然获得。此次研究的最大亮点在于,团队没有把组装过程中的不均一性视为缺陷,而是把它变成了“设计工具”:通过调控软模板内外硅化速率差异,使外层优先固化,中间区域随后塌陷,最终让纳米盘自发转变为环形结构。! r. Q$ I9 W& b, h/ c
研究显示,这种纳米环不仅“长得特别”,而且“跑得更远、钻得更深”。与传统球形颗粒相比,它在体内循环时间更长、肝脾清除更低,同时具备更强的肿瘤外渗和深部穿透能力,肿瘤富集提升达 173%。其原因在于,纳米环中心空腔和特殊曲率改变了其与细胞膜的相互作用方式,使其更不易被免疫系统快速清除,也更容易在致密肿瘤组织中持续推进。& q2 }# y, f& e. P" {
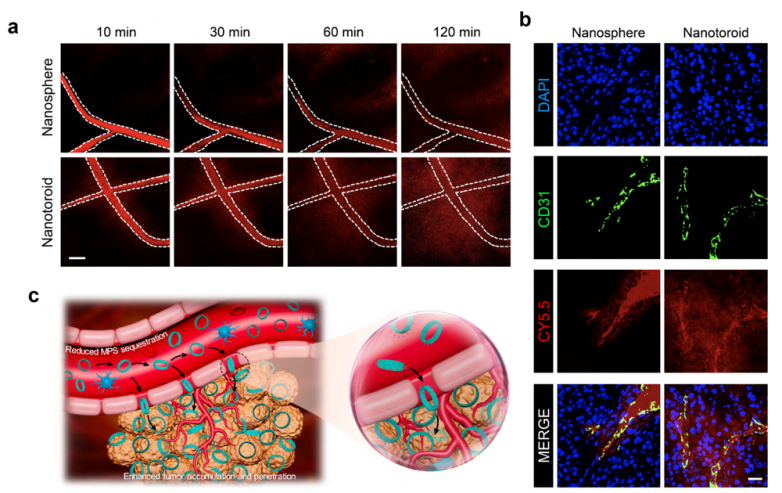 图2 环形拓扑增强肿瘤外渗与组织穿透
图2 环形拓扑增强肿瘤外渗与组织穿透
% W- q4 d$ T6 ]7 E0 [/ H; S( G 在小鼠皮下瘤和脊柱转移瘤模型中,这种智能纳米环展现出良好的治疗前景,尤其在难渗透病灶中表现亮眼。研究表明,材料的拓扑结构本身就可以成为精准调控体内递送和肿瘤穿透行为的重要设计维度。这也意味着,未来肿瘤精准治疗材料的竞争,可能不只在于“装什么药”,还在于“长成什么形”。
7 h/ t/ w( ^" u6 w 这项成果为复杂多孔纳米材料、仿生矿化机制和新一代智能肿瘤递送系统的发展提供了全新思路,也展示了中国科研团队在前沿纳米医学领域的原创突破。0 |8 P# G% O0 W( w7 e2 H- X: p$ Z
) P" C2 g3 ~. F, i. `7 J/ h9 \6 c4 d2 t 免责声明:该文章系我网转载,旨在为读者提供更多新闻资讯。所涉内容不构成投资、消费建议,仅供读者参考。
' H: K! p/ b" m/ z0 e1 e, G1 r 5 N/ a: ?$ h; [4 m
【责任编辑:程慧海】 |
|