|
|

2 [3 U9 p o6 y( O6 c
; C6 d, o$ F( f点评 |朱学良(中国科学院分子细胞科学卓越创新中心)、姚雪彪(中国科学技术大学)
6 E, ]2 z* A' L2026年2月18日, 中国科学技术大学生命科学与医学部张凯课题组在Nature期刊在线发表了题为Roles of microtubules and LIS1 in dynEIn transport machinery assembly的研究论文。该研究系统性地揭示了微管与LIS1介导的胞质动力蛋白-1(dynein)运输系统的组装与启动的新机制,这与领域过去十多年盛行的经典模型显著不同。新的发现表明:Dynein运输复合体的组装并不由传统认为的接头蛋白介导,也不发生在以往认为的胞质中,而是直接发生在“再常见不过、以至于被长期忽视”的微管上。研究表明,微管不仅是为运输复合体提供被动的轨道,更是一种主动的介导运输机器的装配平台,而LIS1的介入则重塑了原有的组装过程,并特异性地募集低微管亲和力的dynein分子到微管附近。: N6 \+ o k7 b+ D1 j
 1 A) G+ a! U% L1 a' V* T6 G
1 A) G+ a! U% L1 a' V* T6 G
% s% q4 ]4 s i& i, _
细胞“运输系统”的核心难题# F& m- ]( |* x* l& F
在真核细胞中,大量生命活动依赖于时空上精确而高效的物质运输。线粒体、内质网、溶酶体、高尔基体、自噬体、细胞核、RNA-蛋白复合物、各类囊泡、蛋白聚集体,以及细胞骨架及骨架蛋白自身等,都需要在特定时间被运送到特定位置。承担这一关键任务的核心动力来源之一,是骨架分子马达,其中胞质动力蛋白-1负责细胞内几乎所有的沿着微管的负向运输过程。Dynein在细胞中的作用就如同汽车等交通工具对人类日常生活的影响一样重要,广泛参与神经发育、免疫极化、蛋白质清除、精子形成、纤毛运动和胚胎发育等几乎一系列关键过程,也关键性地负责病毒等病原体在宿主细胞中的长距离定向运输。鉴于其对大量基本生命活动至关重要,dynein自身或其辅因子的功能障碍与多种神经退行性疾病、发育异常及免疫缺陷密切相关。5 ?& S4 _3 `( r2 p
 5 s+ p4 x, p" a! H
5 s+ p4 x, p" a! H
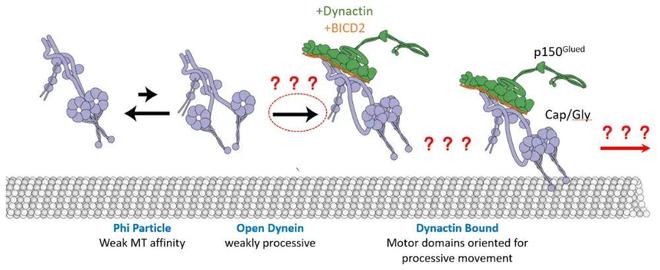
( }) q+ x! J) O; b* V图1:Dynein由自抑制的“Φ粒”被激活为DDA复合物的总体机制。红色问号表示这些过程的深入机制有待进一步研究。! k7 C/ {& G) x) S" o& x
然而,dynein 本身处于两级自抑制状态(Cell 2017):(1)单独的dynein主要以一种被称为“Φ粒”子的状态存在,处于自锁状态,无法完成机械化学循环,也无法结合微管;(2)即使dynein可以自发或受到辅因子调控打开,开放态的dynein无法处于稳定的平行构象,不能有效做持续性的单向运输,只能处于极低程度的运动活性。只有与激活因子 dynactin 及货物适配蛋白(adaptor)组装形成 dynein–dynactin–adaptor(DDA)三元复合体后,才能实现高效、持续的运动。因此,一个核心问题始终困扰着该领域:dynein驱动的细胞运输机器如何组装并启动的?1 @0 p; f/ x) L" }$ ]3 H) D5 @
一个长期存在的困惑:组装效率为何如此矛盾?% t; s7 \8 X u9 a9 w5 u
传统模型认为,DDA 复合体首先在细胞质中完成组装,然后整体结合到微管上启动运输。然而,这一模型存在明显问题:在体外条件下,复合体组装效率极低(~3%),往往需要大量 adaptor 或非生理条件才能观察到稳定复合物。因为dynein样品本身就是属于特别难对付的那种类型,这种极低的组装效率在过去往往被简单地认为 “样品性质不好”。然后,研究人员通过系统性实验,发现事情远非如此,即便得到几近完美的样品也是同样的behavior。这一现象与其在细胞内高效、快速的运输形成鲜明对比,也提示研究人员重新思考:是不是DDA复合物在胞浆中本来就是这种效率?或adaptors介导的组装途径压根就不是它的主要形式,亦或者细胞中极有可能存在不同的组装路径。
5 @, J; {9 o: U# A* N5 j太显而易见了,以至于被长期忽视的“主角”——微管- b+ s5 t) z; M |
研究人员系统重构了DDA复合物的体外组装过程。结果发现,在没有微管的条件下,即使使用高亲和力接头蛋白,溶液中三元复合物形成比例仍仅约3%,且这一低效率在不同核苷酸条件下均保持一致。相比之下,在微管存在时,复合体组装效率显著提高,并表现出明显的核苷酸依赖性。
: M1 f5 w2 [' J1 j0 m进一步定量分析显示,随着微管浓度增加,更多dynein–dynactin(DD)复合物结合到微管上。在非水解型ATP条件下,多达约80%的dynein以DD形式结合微管;即使在通常认为亲和力较低的ATP或ADP·Vi条件下,也能观察到稳定装配。电子显微镜分析进一步表明,在混合体系中形成的三元复合物几乎全部定位于微管上。) z" K+ B! A* G7 y
为验证这一现象的普遍性,研究团队对多种已报道的接头蛋白进行了系统测试,包括BICDR1、BICD2、HOOK3、RILP、SPDL1、JIP家族和HAP1等。结果显示,在缺乏微管时,大多数体系中仍以分离状态的dynein和dynactin为主,而三元复合体形成极为有限。这表明,微管是介导运输复合体组装的关键因素,不仅仅只提供被动轨道。
/ _( l8 o, M6 s新的组装机制:微管先行,而非接头蛋白驱动
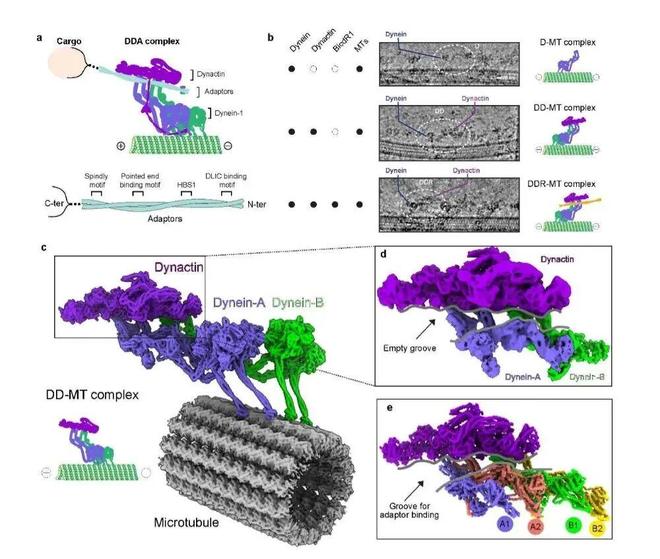
1 M1 g5 Q* u& ~! I5 ^3 c传统模型认为,接头蛋白首先介导dynein与dynactin结合,并关键性地决定了dynein-dynactin的化学计量(例如BICDR1和BICD2分别介导2个和1个dynein分子结合dynactin,Nature 2018)。新的研究结果则显示,与传统认知刚好相反,dynein在结合微管后即可发生关键构象变化,其马达结构域自动排列为平行状态,并进一步诱导尾部区域形成有利于dynactin结合的构象,从而高效形成DD复合物。特别的,结合微管后的dynein-dynactin复合物始终自发呈现稳定的2:1化学计量比,且这一过程完全不依赖于接头蛋白。这一发现表明,dynein运输系统是优先在其行走的“轨道”微管上直接形成的,而在胞质中的接头蛋白并非其初始装配的决定因素。
" i' r' U& {: d) ?/ _
 : k' I4 y {0 E6 i5 T- E
: k' I4 y {0 E6 i5 T- E
, y. q3 d# v" p5 O8 c. `0 K+ z- d: h. a
图2:DDA组装复合体在微管上的模型图、不同状态的冷冻电镜检查,以及没有接头蛋白的情况下的DD-MT高分辨结构。+ l+ x. @7 m# }
接头蛋白的动态进入与交换7 h8 A7 r5 f" A
在新的框架下,一个关键问题是接头蛋白如何结合到已形成的微管结合DD复合物中。实验结果显示,无论是先在溶液中预组装后再加入微管,还是先在微管上形成DD复合物再加入接头蛋白,均可成功形成DDA复合体。这说明接头蛋白能够在DD复合物形成后再结合。更深入的动态结构和生化分析表明,DD复合物存在一种特殊的动态构象波动,可在特定状态下开放关键结合位点,从而形成一种 “动态门控”机制,允许接头蛋白直接进入在微管上的DD复合物。进一步的微管上竞争性实验表明,不同接头蛋白可以在微管上对同一DD复合物进行替换,高亲和力接头能够取代低亲和力接头,而无需复合体彻底解离。这一机制成功解释了细胞中长距离运输过程中接头蛋白的阶段性交替,而传统模型则和这些现象相悖。
6 T0 {) R7 O- Y研究人员进一步探讨了adaptors是如何被招募到微管结合的DD复合物上。结果发现,多数adaptors一个关键结合区域CC1 box处于自抑制状态,被一段类似于dynein中轻链(LIC)的螺旋结构所占据,形成一种“自我封闭”(self-locked)的构象。去除这一抑制螺旋后,adaptor与DD复合物的结合亲和力明显增强。然而,如果进一步将整个CC1 box区域删除,反而会显著降低结合能力。值得注意的是,这一现象在先于微管和微管结合后(post-MT)再招募的两种条件下均一致,说明CC1 box既受到自抑制调控,又是实现稳定招募所必需的关键结构元件。( ? }5 W( z% N; d9 ?
视频1:Dynein中轻链LIC介导的adaptor招募机制。特别地,冷冻电镜结果揭示这两条用于捕获adaptors的LIC的C端需要来自两个不同的Dynein二聚体各贡献一条。这进一步暗示了2:1的DD复合物是招募adaptors的先决条件,而不是相反的机制,并且2:1化学计量是微管诱导的内在形式,与adaptors无关。
( S/ e0 f* S7 z8 @& h: b4 _+ c& E微管上的接头交换:长距离持续运输成为可能
/ K* |& v7 I- N- v5 P8 j( F7 `如果 adaptor 能够“挤入”已形成的微管结合 DD 复合物,那么也就存在一种可能性:接头蛋白有可能在该复合物不被彻底解聚的前提下,也是可以在DD种与其它接头相互交换的 (exchangeable)。 R+ n g: x6 W+ g; p
为验证这一假设,研究人员设计并进行了一个“微管上的竞争实验” (on-microtubule competition assay)。简单说,研究人员首先在微管上组装形成 DDK 复合物,这是比较弱的一直DDA complex,随后向沉淀中加入含有 BicDR1 的溶液。同时还并进行了反向实验,即先组装 DDB,再加入 Track2。凝胶结果清楚显示:BicDR1 能有效置换 Track2 进入 DD 复合物,而由于亲和力较低,Track2 几乎无法竞争性地置换 BicDR1。不过,当删除了 Track2 中的自抑制螺旋 (autoinhibited helix),从而增强其结合亲和力后,Track2 即可在一定程度上与 BicDR1 进行竞争,实现在微管上的部分置换。6 F2 x0 z# Z4 j# q
 7 [$ g4 S0 A' o- m/ j( z0 ]3 Z
7 [$ g4 S0 A' o- m/ j( z0 ]3 Z
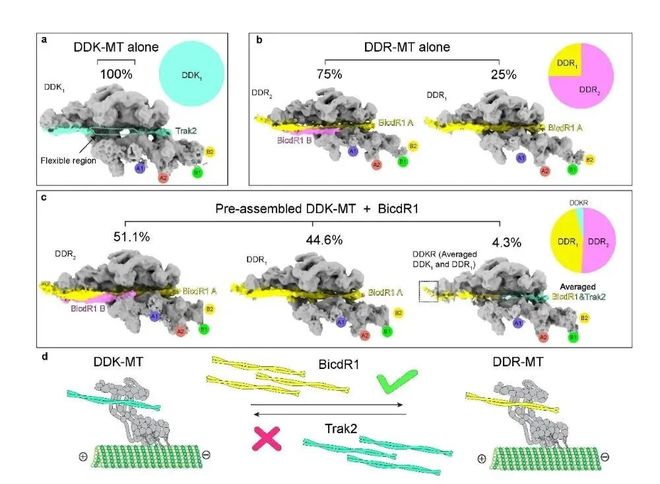
6 |; C2 }4 [( f; K; z+ S( i图3:冷冻电镜结果直接“看到”不同亲和力的adaptors可以直接在预组装的DD-MT复合物内部直接竞争交换,与生化结果相互印证。
7 ]; |/ j/ b; P% `* z' G3 F研究人员进一步进行了 冷冻电镜 (cryo-EM) 分析,以定量观察 微管上 adaptor 竞争置换过程中的结构变化。结果与凝胶实验的观察高度一致。研究首先获得了微管结合态的DDK和DDR复合物并对两种不同亲和力的DDA复合物进行结构比较。在预组装DDK–微管复合物后,加入 BicDR1 所获得的结构,很明显,大多数复合物已经转变为 DDR,仅有少数例外仍保留为 DDK。和凝胶果一直,反过来用DDK来竞争已经形成好的DDR则不行。( \* O3 Z3 k" o/ J6 _* ?
LIS1:扩展组装过程,而非产量
# k/ k) y! h, C/ t长期以来,LIS1被认为是促进dynein激活和DDA复合体形成的关键因子,其真实作用机制一直不清,甚至不同研究结果在特定情况下相互矛盾。本研究发现,在相对干净的体系中,遵循单一因子变量原则,系统性地验证了无论在溶液还是微管上,LIS1几乎不会显著增加最终DDA复合体的产量,表明其作用并不体现在形成更多复合体的“数量”层面。* X8 n1 w" w7 y1 r5 q! j
. Z* W8 Q7 N2 a! f0 F
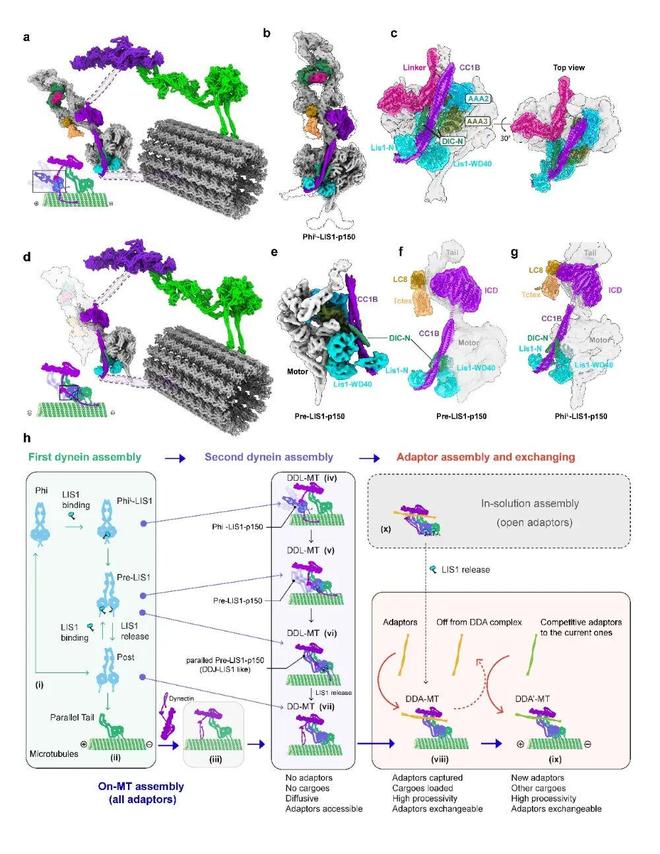
# V+ J! n+ s; G1 P: x$ F8 Q3 F图4:动态冷冻电镜分析揭示了LIS-p150介导的弱微管亲和力的dynein分子捕获机制。
; J1 D) I( g0 d; x: I1 w" l进一步的结构、生化和单分子分析显示,LIS1的核心功能在于调控组装“过程”:它能够稳定多种组装中间体,扩展组装的构象空间,并特异性标记处于低微管亲和力状态的dynein分子。与此同时,dynactin上的长而柔性的p150结构可从微管上的预组装DD复合体伸出,像“章鱼触手”一样特异性地捕获这些被LIS1标定的低微管亲和力的dynein,实现动态募集;而当dynein稳定结合微管形成平行构象后,微管结合导致的变构效则迫使LIS1从dynein上解离。
* n( A3 l% z, Y! i自此,研究人员证明LIS1真正的作用并不是增加最终的运输复合体量,而是通过重塑组装路径、提高动态招募效率,并在运输过程中增强其灵活性和动力学性能。这一结果清晰地区分了“量”与“过程”混淆导致的误区,协调了领域内长期存在的争论。
9 g6 @" c: S. t& Q
* W! F. `& h: F6 _- N {, I1 K
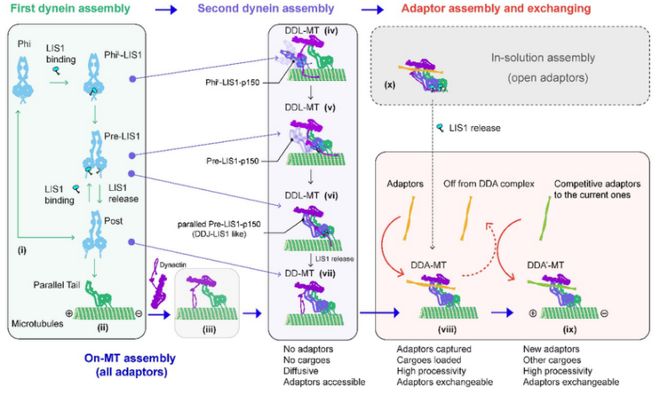
; T- ], H! Y# j$ ^8 _图5:本研究对dynein运输复合体组装的新机制系统性总结和更新。关于经典模型部分(x)因其仅占整个组装效率的3%左右并在以往文献中有更详细解释,所以在本图中省略。/ A2 s# m) N' h4 O& M& J' X3 N
中科大生命科学与医学部张凯教授为本研究的通讯作者,南京医科大学饶钦辉教授(张凯实验室前博后,兼本论文共通讯)及中科大张凯实验室杨俊特任副研究员为文章共同一作。张凯实验室前博士生柴鹏鑫博士(现为哈佛大学博士后)发展的微管结合态运输复合体的高分辨cryo-EM方法对本研究有关键推动作用,科罗拉多州立大学Steven Markus教授在DDA组装效率方面给予了重要协作。! {7 E7 p, t b1 v( H, ?8 L+ l
原文链接:https://www.nature.com/articles/s41586-026-10153-y: [7 Z; e: G! F6 m( g
张凯实验室长期从事高分辨原位成像、细胞骨架及骨架马达蛋白、胞内物质运输、细胞运动、能量代谢,并致力于融合经典分析+AI+高性能计算赋能的全尺度高分辨细胞结构组学等前沿方向。在原位技术和大规模细胞结构组不断完善成熟的基础上,实验室亦重点关注并长期致力于发展相关技术在新型诊断、疾病早筛和健康管理等方向的潜在重大医疗应用,欢迎对相关研究方向感兴趣的各个领域的理工学科的优秀学生、博后及青年学者加盟。! J4 R5 o& V# n2 k/ J: h
2 Z2 P0 Q, G3 K6 r0 O简历投递( 有意者请将个人简历等材料发至 ):
4 Z4 }6 M0 T/ k) @5 v0 c+ Q7 b9 Xhttps://jinshuju.net/f/ZqXwZt或扫描二维码投递简历+ k! q! U$ R) e

/ i8 i/ I/ Q1 Q" F* X0 H! y; u5 M
7 D- B6 I- m' m3 n专家点评
& G' A8 W! x7 D! i# L7 ]朱学良(中国科学院分子细胞科学卓越创新中心/生化与细胞所 教授/研究员)
1 n& A) t0 D) H* E- j细胞犹如城市,需要通过各类交通运输来帮助维持稳态和行使功能。胞内运输所用的“车辆”是被称为分子马达(molecular motor)的蛋白质复合物[1],而“公路”则是细胞骨架微管和微丝。分子马达通过结合细胞器等“货物”并水解腺苷三磷酸(ATP)以化学能驱动构象变化,使其两条重链(heavy chain)的马达结构域如双腿般交替沿微管或微丝行走,实现运输功能。分子马达也行使牵拉功能,在细胞分裂、细胞迁移、肌肉收缩等过程中发挥作用。
$ S& m$ s$ i, V. w5 y i6 T# R) w细胞内的长途运输主要由胞质动力蛋白(cytoplasmic dynein)和驱动蛋白(kinesin)这两类微管依赖性分子马达来完成[2, 3]。它们分别朝向微管的负端和正端运动,介导负向和正向的运输。驱动蛋白以众多的种类来适配不同的货物,结构相对简单,而胞质动力蛋白只有两种,因此其组成、结构和调节机理尤为复杂。其中,胞质动力蛋白1(dynein-1)可通过更换不同的接头蛋白(adaptor)而结合不同的货物,负责了胞体内几乎所有货物的负向运输。它不仅拥有长度超过四千氨基酸的两条重链和多条中链、中轻链、轻链,还处于双重自抑制状态,需要逐步解除自抑制,并与由二十多个亚基组成的动力蛋白激活蛋白(dynactin)和一种接头蛋白形成三元复合物(DDA复合体),才成为能在微管上持续行走的活性形式[2]。如此复杂的生物纳米机器究竟如何实现自组装是个长期被关注的重要科学问题,但由于研究技术和方法的局限,进展缓慢。近年来,随着冷冻电镜技术在解析复杂蛋白质复合物的精细结构方面显示出越来越强大的能力,才得以打破僵局。耶鲁大学/中国科技大学张凯教授研究组的在Nature刚发表的研究发现,即主要采用冷冻电镜技术,揭示了DDA复合体组装的全新机理并修订了领域内的认知。
8 G7 O& d# c$ P( Y$ x前人的研究提示接头蛋白先在胞质中介导DDA复合体形成,且接头蛋白的种类决定了DDA中Dynein-1和Dynactin的分子比(2:1或1:1)[4]。然而,张凯组发现纯化的猪细胞内源dynein-1即能单独在微管上形成有利于Dynactin结合的开放构象,且能和Dynactin在微管上高效组装成具有2:1分子比的二元DD复合物。该DD复合物能够进一步招募各种的接头蛋白形成DDA复合体。而且,高亲和力的接头蛋白还可以竞争性替换DDA复合体中的低亲和力接头蛋白。由于微管在细胞内分布广泛,且与DD复合物的表观亲和力比接头蛋白要高出约5倍,这一全新的微管依赖性组装模型更像是反映了细胞内DDA复合体的主要组装机制。相比之下,接头蛋白介导的组装效率很低,即使在细胞内能发生,也只可能是次要机制。同时,新模型可轻松解释诸如Dynein-1在从神经轴突末端向胞体运输自噬体的过程中会更换不同的接头蛋白的现象[5]。/ d1 h# t2 k- H! r E
张凯组还进一步探究了LIS1在DDA复合体组装中的作用。LIS1因其基因突变导致人类大脑缺乏脑回(无脑回征,lissencephaly)而得名,其与Dynein-1的联系可追溯到90年代其同源蛋白NudF与Dynein-1属于影响构巢曲霉(Aspergillus nidulans)菌丝内细胞核迁移的同一个遗传通路的研究发现[6, 7]。我实验室曾通过一系列研究率先证明该通路的另一成员NudE[8]在哺乳动物中的同源蛋白Nudel和NudE (后来被改称NDEL1和NDEl)及其与Dynein-1和LIS1的结合,是Dynein-1在胞内运输和有丝分裂中的活性所必须的[9-13],但尽管有多方后续研究[14],精细可信的分子机理直到最近才被张凯组及其合作者阐明:LIS1促进Dynein-1分子解除第一重自抑制构象,而NDE1则促进LIS1与自抑制Dynein-1的高效结合[15, 16]。在这篇Nature论文中张凯组进一步发现,LIS1并不促进更多DDA复合体的形成,而是通过标记低微管亲和力的Dynein-1、稳定中间态等提高DD复合物中第二个dynein-1分子的招募效率,促进DDA复合体的快速形成。
- Z: D& C7 f" [2 O# P2 y q% e张凯教授研究组这些系统性的研究发现令人信服,可望对深入解析Dynein-1介导的细胞活动的分子机理产生深远影响。同时,也让人对其它动力蛋白的功能复合物的装配机理浮想联翩。另一种胞质动力蛋白(cytoplasmic dynein-2)的功能是介导鞭毛/纤毛内的物质运输(intraflagellar transport, IFT),它结合IFT复合物而非Dynactin和接头蛋白,并进一步组装成“IFT列车”行使功能[17, 18]。此外,还有8种动力蛋白被锚定在轴丝微管上(因而叫做轴丝动力蛋白,axonemal dynein),驱动鞭毛/纤毛的快速摆动,其中7种只有一条“腿”[18]。尽管目前对相关装配机理也有深刻认识[17, 19],但均未涉及微管的贡献。“剧情”将来是否也会出现大反转呢?我们拭目以待。. R! E* P1 M; z+ V* G
专家点评; v! s+ @5 r' s- o- S
姚雪彪(中国科学技术大学)+ Z9 m7 t( N# \. z1 \4 F
利用冷冻电镜单颗粒技术与新的解析方法相结合,张凯团队在微管马达蛋白dynein复合体的构-效关联研究方向做出了一系列创新性发现。他们这项最新研究改变了我们对在马达蛋白在胞内运输的传统认知,具有范式变革的意义。长期以来,领域普遍认为dynein运输复合体主要在胞质中由接头蛋白(adaptors)介导整个机器的组装,而该工作系统证明,微管本身才是运输机器的关键装配平台,能够主动促进dynein–dynactin复合体的组装、构象重排及化学计量比,并在不依赖adaptors。这一发现将微管从传统意义上的“被动轨道”提升为“主动组织者”,从根本上改变了我们对dynein驱动的胞内运输体的启动机制的理解。
. n \2 h9 m: b h& _( I/ G此项研究同时更新了我们对LIS1分子功能本质的传统认知:其主要功能并非直接增加运输复合体的最终产量,而是稳定组装中间体、扩展构象空间并促进低亲和力dynein的动态募集,从而实现对组装及运输过程的动态调控。这一新购效概念的建立为深入理解dynein调控机制提供了新的统一框架。
% m# j+ `7 a; X5 v9 M' J; T: g尽管该研究在方法上主要基于体外重组体系,但全文核心始终围绕细胞生物学问题,并逐步深入地回答细胞是如何在特定的时间和空间启动运输机器。例如,文章中清晰地阐明了adaptors是如何动态进入在微管上预组装的dynein-dynactin,以及如何在复合物不解聚的前提下实现adaptors的交换机制,为神经系统中的高效的长距离运输过程给出重要见解。正如论文评审专家所说,这项工作“非常出人意料,将在该领域乃至整个细胞生物学界引起广泛关注”。, |; l* u! D5 d+ x( J) c
总体而言,该研究将分子机制研究紧密连接到胞内运输层面的调控逻辑之中,对理解dynein蛋白质机器在细胞极性建立、神经发育、胞内运输及相关突变体驱动相关疾病演进机制具有重要意义,我们期待高时空分辨dynein运输复合体调控胞内运输快照(snapshot)的诞生。
' m9 x/ I( q( y2 P! s6 k& X制版人: 十一3 E- _' W$ U5 |# ^5 W
参考文献:3 o( Z8 k( {: y6 A& T
1.Vale, R.D., The molecular motor toolbox for intracellular transport. Cell, 2003.112(4): p. 467-80.
* _; `8 O7 j% t8 c- [" }2.Reck-Peterson, S.L., et al., The cytoplasmic dynein transport machinery and its many cargoes. Nat Rev Mol Cell Biol, 2018.19(6): p. 382-398.
. h' } D! m" @' L) Q3.Yildiz, A., Mechanism and regulation of kinesin motors. Nat Rev Mol Cell Biol, 2025.26(2): p. 86-103.- c" C6 s/ q# \/ E, m: t, z3 T
4.Urnavicius, L., et al., Cryo-EM shows how dynactin recruits two dyneins for faster movement. Nature, 2018.554(7691): p. 202-206.
X" T; r: w! Z( V5.Cason, S.E., et al., Sequential dynein effectors regulate axonal autophagosome motility in a maturation-dependent pathway. J Cell Biol, 2021.220(7).2 [* D; B1 t# H6 o1 Q2 |
6.Xiang, X., S.M. Beckwith, and N.R. Morris, Cytoplasmic dynein is involved in nuclear migration in Aspergillus nidulans. Proc Natl Acad SCI U S A, 1994.91(6): p. 2100-4.2 p. v H( H8 [: N4 N, F( a3 L9 x
7.Xiang, X., et al., NudF, a nuclear migration gene in Aspergillus nidulans, is similar to the human LIS-1 gene required for neuronal migration. Mol Biol Cell, 1995.6(3): p. 297-310.
, ], q3 ~3 T% j: E- A/ c2 c3 M+ f8.Efimov, V.P. and N.R. Morris, The LIS1-related NUDF protein of Aspergillus nidulans interacts with the coiled-coil domain of the NUDE/RO11 protein. J Cell Biol, 2000.150(3): p. 681-8.7 w X) I9 y6 D
9.Liang, Y., et al., Nudel functions in membrane traffic mainly through association with Lis1 and cytoplasmic dynein. J Cell Biol, 2004.164(4): p. 557-66.
1 E7 \3 L f' b: z10.Zhang, Q., et al., Nudel promotes axonal lysosome clearance and endo-lysosome formation via dynein-mediated transport. Traffic, 2009.10(9): p. 1337-49.+ _6 h# D: r6 ?: s3 a
11.Liang, Y., et al., Nudel Modulates Kinetochore Association and Function of Cytoplasmic Dynein in M Phase. Mol Biol Cell, 2007.18: p. 2656-2666.
c8 b2 p$ u- I( j' ~; i# |12.Yan, X., et al., Human Nudel and NudE as regulators of cytoplasmic dynein in poleward protein transport along the mitotic spindle. Mol Cell Biol, 2003.23(4): p. 1239-50.
4 b5 F9 Q# N) M- Z# Z( z: Q |& S13.Li, Y., et al., Kinetochore dynein generates a poleward pulling force to facilitate congression and full chromosome alignment. Cell Res, 2007.17(8): p. 701-12.6 G5 S. ^+ ~3 k d y7 Q
14.Garrott, S.R., J.P. Gillies, and M.E. DeSantis, Nde1 and Ndel1: Outstanding Mysteries in Dynein-Mediated Transport. Front Cell Dev Biol, 2022.10: p. 871935.
( e' g* Y2 f$ ]9 A4 w5 d* o15.Geohring, I.C., et al., A nucleotide code governs Lis1's ability to relieve dynein autoinhibition. Nat Chem Biol, 2026.; b2 U3 u$ o9 V- _* m) B9 f1 B1 b
16.Yang, J., et al., Nde1 promotes Lis1 binding to full-length autoinhibited human dynein 1. Nat Chem Biol, 2026.22(2): p. 274-283.% a$ f+ W) A3 `, i- T" b6 i; O
17.Lacey, S.E. and G. Pigino, The intraflagellar transport cycle. Nat Rev Mol Cell Biol, 2025.26(3): p. 175-192.
, M# o' X" ~. l18.Klena, N. and G. Pigino, Structural Biology of Cilia and Intraflagellar Transport. Annu Rev Cell Dev Biol, 2022.38: p. 103-123.
" G( q5 l3 S' Z$ |0 w' _19.Qiu, T. and S. Roy, Ciliary dynein arms: Cytoplasmic preassembly, intraflagellar transport, and axonemal docking. J Cell Physiol, 2022.237(6): p. 2644-2653.% x4 p2 i, d* a7 v" C3 Q
学术合作组织: _5 ]& \) T# N# M$ Z
(*排名不分先后)6 g2 O$ Q5 Y+ e* J

, x0 k3 t; d# U. q
3 R7 c. z: t. a4 B3 s9 q. T9 X* l- {6 H- a n, \* o, k
战略合作伙伴6 b9 I2 ?: ]" \9 D+ W+ z
(*排名不分先后)
5 s, D( l0 Q1 B

. f" U9 F: x6 U
* N/ m# v# i4 k1 J/ X& \1 R

) w: `- W2 y7 R0 l3 K/ m. o& p" ~5 j; F+ a& `9 Q* X* _. w
转载须知/ ?4 t$ K, z( p" {& g# F
, `- S+ G! m1 H6 c4 c6 m$ b【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。 f5 z1 |% u& K$ L" @" N
BioArt" W1 s: W% s5 ]+ Z$ `- g3 L1 ]
Med% M7 @& j9 l! V% u: N9 ~
Plants) o0 }2 J) S+ O# H. Q$ C6 Q
人才招聘
. P% ~+ t' C1 p3 `近期直播推荐9 P c5 E% F( t$ v0 l

" g& B( |$ J. J4 e
: L! E% q) I1 z. l5 \% \( ~ d点击主页推荐活动4 V& f6 [. k: E1 Z3 C) p
2 g! v3 ^- X" V. R. A关注更多最新活动!
( K/ p1 l' x! |" ~2 _5 d# C4 F
) z& I: ~5 i7 g% }0 o( h

|
|